Snadná doprava léčiv přímo do buněk je jedním z velkých cílů farmaceutického průmyslu. Procesům, které probíhají v buněčné membráně a jsou zodpovědné za transport látek do buňky a z buňky ven přitom stále z velké části nerozumíme na detailní molekulové úrovni. Vědecký tým Pavla Jungwirtha z Ústavu organické chemie a biochemie AV ČR (ÚOCHB) ve spolupráci s kolegy z Česka a Německa nyní objevil dosud neznámý mechanismus, jak se mohou do buněk dostat krátké peptidy, které by v principu mohly sloužit jako nosiče molekul léčiv. Výsledky jejich výzkumu nyní publikoval prestižní mezinárodní vědecký časopis Proceedings of the National Academy of Sciences of the USA.
Schopnost krátkých, kladně nabitých peptidů pronikat do buněk byla poprvé pozorována při studiu HIV a dnes se začíná využívat k transportu léčiv do buněk. Doposud se ale využívalo toho, že k transportu dochází primárně formou tzv. vezikulárního transportu, tedy prostřednictvím transportního váčku (vezikuly) oddělujícího se z buněčné membrány a obepínajícího přepravovanou látku. Ta se po transportu do buňky musí z váčku opět uvolnit, což může představovat technickou komplikaci pro efektivní dopravu léčiva. Je ale známo, že peptidy se mohou do buněk dostávat i pasivně, tedy bez energetické asistence ze strany buňky. Přesný mechanismus však až dosud popsán nebyl.
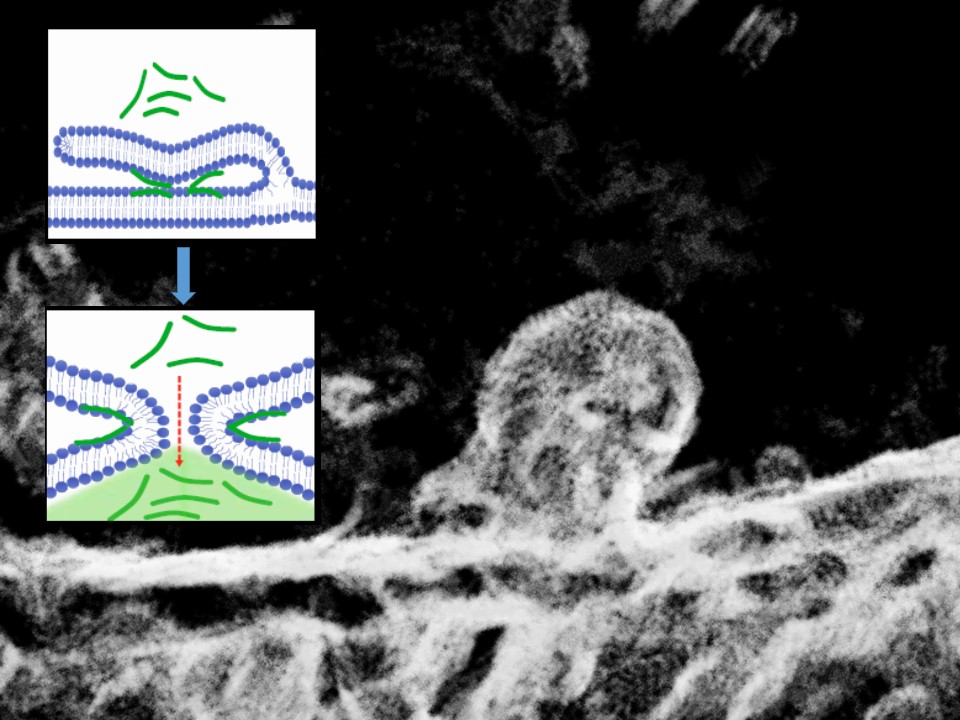
Vědci vedení Pavlem Jungwirthem nyní pomocí fluorescenční a elektronové mikroskopie v kombinaci s počítačovými molekulovými simulacemi odhalili dosud nepopsaný pasivní mechanismus dopravy kladně nabitých peptidů do buňky. Ten je založený na splynutí (fúzi) membrán vyvolaném samotnými transportovanými peptidy (viz obrázek).
Vědci tak ukázali, že proces pasivního přenosu nabitých peptidů do buněk a obecně známý proces membránové fúze, indukované například vápenatými ionty v neuronech při přenosu nervového signálu, mají společný mechanistický základ – jsou to obrazně řečeno dvě strany téže mince.
„O praktickém využití tohoto objevu lze zatím jen spekulovat,“ říká Pavel Jungwirth. „Pokud se ale nově objevený mechanismus prokáže jako dostatečně robustní, dalo by se v budoucnu uvažovat o možnosti pasivního transportu molekul léčiv do buněk bez potřeby je následně uvolňovat z vezikulí, které při tomto procesu prostě nevznikají.“
Pavel Jungwirth se se svou skupinou dlouhodobě zaměřuje na odhalování zákonitostí molekulových procesů probíhajících v buněčné membráně, které jsou nám dosud z velké části neznámé. Lepší porozumění základním dějům probíhajícím v membránách buněk našeho těla otevírá postupně nové možnosti kontrolování těchto procesů a tím potenciálně i efektivnější způsoby dopravy molekul léčiva na místo účinku.
Článek:
- Christoph Allolio, Aniket Magarkar, Piotr Jurkiewicz, Katarína Baxová, Matti Javanainen, Philip E. Mason, Radek Šachl, Marek Cebecauer, Martin Hof, Dominik Horinek, Veronika Heinz, Reinhard Rachel, Christine M. Ziegler, Adam Schröfel, Pavel Jungwirth. Arginine-rich cell-penetrating peptides induce membrane multilamellarity and subsequently enter via formation of a fusion pore. Proceedings of the National Academy of Sciences Nov 2018, 201811520; DOI: 10.1073/pnas.1811520115
Obrázek:
Bifurkace buněčné membrány zachycená v elektronové mikroskopii a molekulové schéma procesu. (Kredit: ÚOCHB)